[논문 리뷰] Artificial intelligence-enhanced risk stratification of cancer theraputics-related cardiac dysfunction using electrocardiographic images
0. 논문 선정 이유
- 현재 하고 있는 연구 중 하나가, 심전도(ECG) 데이터를 활용하여 LVEF를 예측하는 인공지능 모델을 개발하는 것인데, 모델 개발은 마무리되었고, 이를 어떻게 실제 임상 현장에 (구체적으로 어떤 환경/환자/상황 등에) 적용할 수 있을지 고민을 하고 있는 중이다. 따라서 해당 논문을 읽으며 추후 방향성에 대한 힌트를 얻을 수 있을 것으로 기대되어 선정하게 되었다.
- 해당 논문의 내용을 이해하기 위해서는 기본적인 의학 개념에 대한 이해가 필요할듯! (본문 1-2 ~ 1-4 참고)
1.Introduction
1-1. Cancer Therapeutic-Related Cardiac Dysfunction (CTRCD)

- 몇몇의 암 & 종양 관련 치료법들은 장기적으로 봤을때 심혈관계에 안 좋은 영향을 끼칠 수 있으며, 이를 Cancer Therapeutic-Related Cardiac Dysfunction (CTRCD)라고 한다.
- 해당 논문에서는 CTRCD를 1) cardiomypathy(심근병증), 2) Heart Failure (심부전), 그리고 3) LVEF가 50 미만으로 떨어지는 경우로 정의한다.
- 현재 각 환자 별 CTRCD가 발생될 위험도에 따라서 효과적인 치료 프로토콜을 설계할 필요성이 제기되고 있고, 특히 암 & 종양 환자에게 치료를 적용하기 전, CTRCD 발생이 예상되는 고위험군 환자를 미리 정확하게 식별하는것이 필요한 상황이다.

- 본 연구는 크게 두가지 목적을 가지고 있다.
1) 심장 초음파 대신 심전도와 인공지능을 활용한 새로운 바이오 마커를 제시하는 것
: 기본적으로 GLS는 심장 초음파 검사를 통해 측정되고, 이 값을 통해 좌심실의 수축 기능 장애를 평가한다. 이때 심장 초음파 대신 조금 더 간편하고 저렴한 심전도를 활용하여 LVSD를 평가해 보자라는 컨셉이다.
2) 인공지능 모델을 활용하여 CTRCD의 위험도를 조기에 예측하는 것.
(해당 논문을 이해하기 위해 필요한 기본적인 의학 지식들 : 1-2 ~ 1-4)
1-2. Heart Failure (HF) & Left Ventricular Ejection Fraction (LVEF)

- 해당 논문에서 CTRCD 중 하나로 정의한 Heart Failure에 대해 간단히 설명하자면,
- 심장은 기본적으로 수축과 이완을 반복하면서 온몸으로 혈액을 뿜어주는 펌핑 역할을 수행한다.
- 이러한 심장이 온몸에서 필요한 만큼의 혈액을 제대로 펌핑하지 못하는 상태를 Heart Failure (심부전)라고 한다.
- 여러 가지 심장 구조들 중에서, 특히 Left Ventricle (좌심실)은 온몸으로 깨끗한 혈액을 내뿜어주는 역할을 하기 때문에 이 부분의 기능이 떨어지면 여러가지 큰 문제들이 발생될 수 있다.
- 따라서 이 좌심실이 혈액을 잘 펌핑하고 있는지에 대한 평가 지표로 'Ejection Fraction'이라는 개념이 있다.
- Ejection fraction은 EDV와 ESV값을 통해 계산된다.
- EDV End Diastolic Volume으로, 심실이 수축하기 직전, 심실에 차있는 혈액의 최대량을 의미한다. 그리고 ESV는 End Systolic Volume으로, 심장이 수축을 마친 시점에 심실에 남아있는 혈액의 양을 의미한다.
- 예를 들어, 심장이 이완했을 때, 심실에 차있는 최대 혈액이 100ml이고, 수축 후 심실에 남아있는 혈액이 40ml라고 했을 때 각각의 값을 위의 수식에 대입해 보면 LVEF는 60%로 계산될 수 있다.
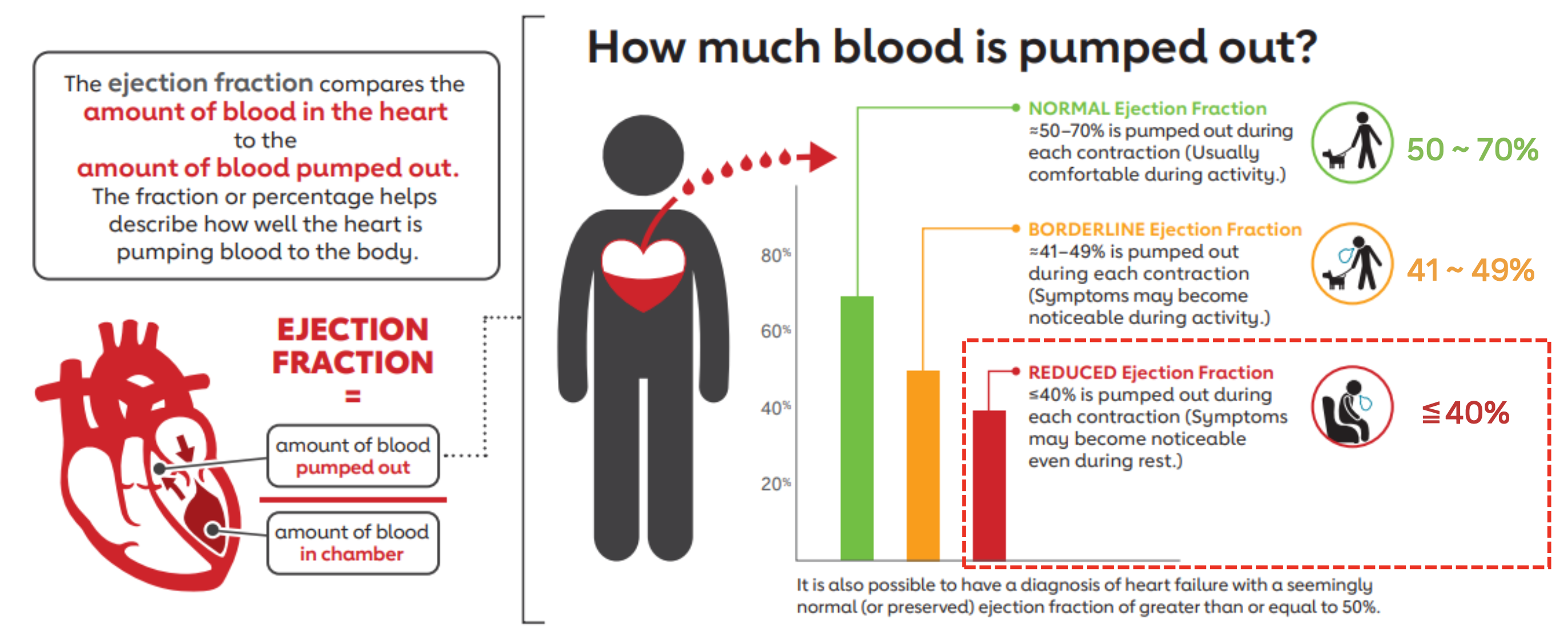
- American Heart Association (AHA)에서 제시된 기준에 따르면, LVEF가 50~70 범위인 경우 정상이며, 만약 40 이하로 떨어지게 되면 좌심실의 기능이 저하된 상태로 간주한다.
1-3. Left Ventricular Systolic Dysfunction (LVSD)
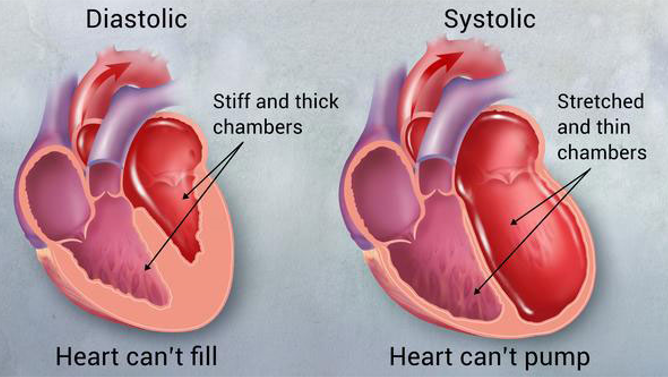
- Heart Failure는 크게 diastolic & systolic dysfunction으로 나눌 수 있다.
- Diastolic dysfunction은 심장 근육이 너무 두껍고 딱딱해져서 심실 안으로 충분한 혈액을 채우지 못하게 되고, 채워져 있는 혈액자체가 많지 않기 때문에 좌심실이 수축하더라도 몸에서 필요한 만큼의 혈액을 공급하지 못하는 상태를 의미한다.
- Systolic dysfunction은 심장 근육이 너무 얇고 약해서 펌핑자체를 못하는 상태를 의미하며, 이를 LVSD라고 한다.
1-4. Global Longitudinal Strain (GLS)
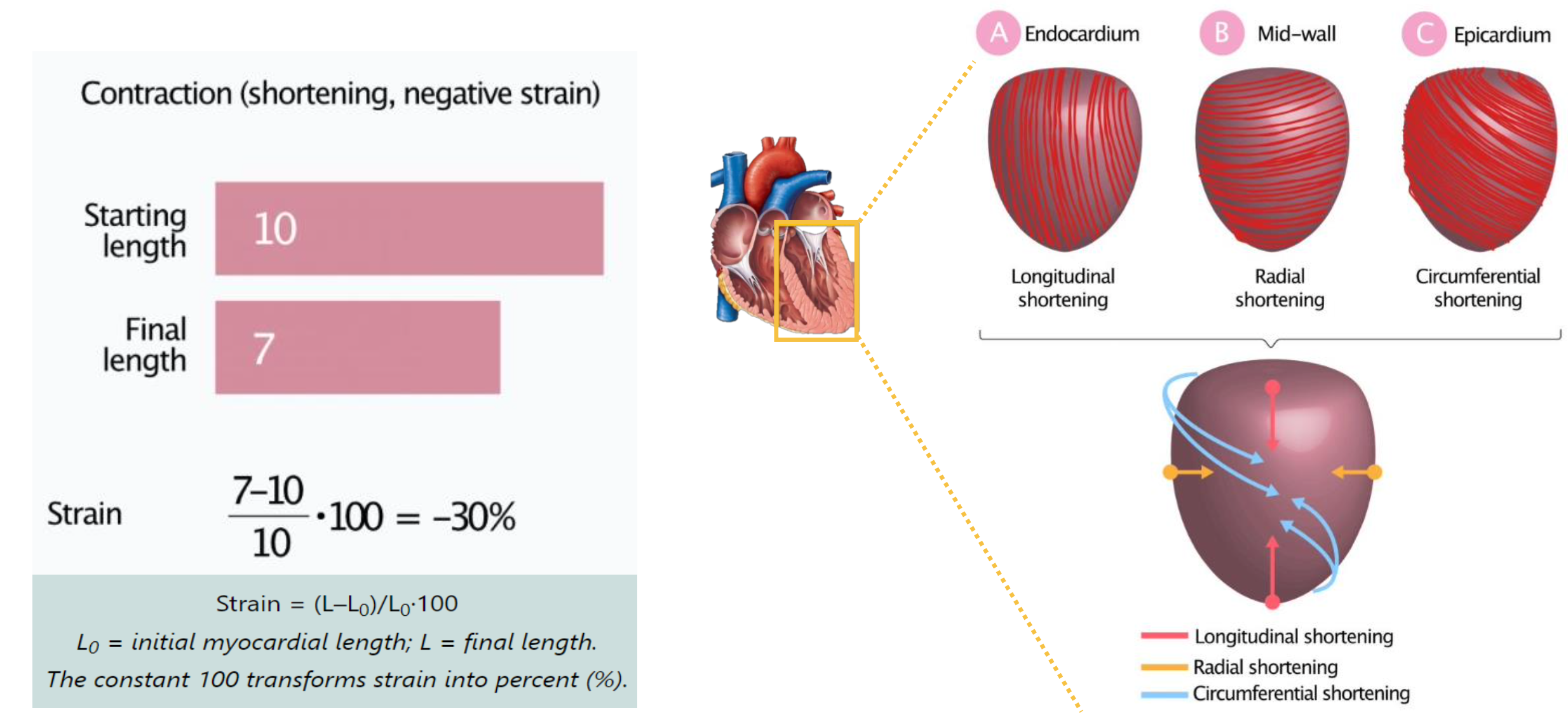
- Global Longitudinal Strain (GLS)는 LVEF와 비슷하게, 심장의 기능을 평가하는 지표이며, 심장 초음파 검사를 통해 측정되는 값이다.
- 보편적으로 심장의 기능을 평가하기 위해 LVEF가 많이 사용되지만, 항암 요법을 시행하는 환자들의 경우, LVEF는 정상범위에 있더라도 GLS는 감소할 수 있다.
- GLS가 LVEF보다 좌심실의 수축 기능 장애를 평가하는 데에 있어 더 민감한 지표라고 할 수 있다.
- GLS의 계산은 (왼쪽의 수식참고) 처음 길이가 10이고, 최종적인 길이가 7이라고 가정했을 때, 최종 변형률은 -30%로 계산된다.
- GLS를 측정할 때, 위의 오른쪽 그림처럼 총 3가지 view를 잡게 되고, 이 세 방향에서 측정된 GLS값을 평균 내어 최종적인 GLS값을 산출하게 된다.
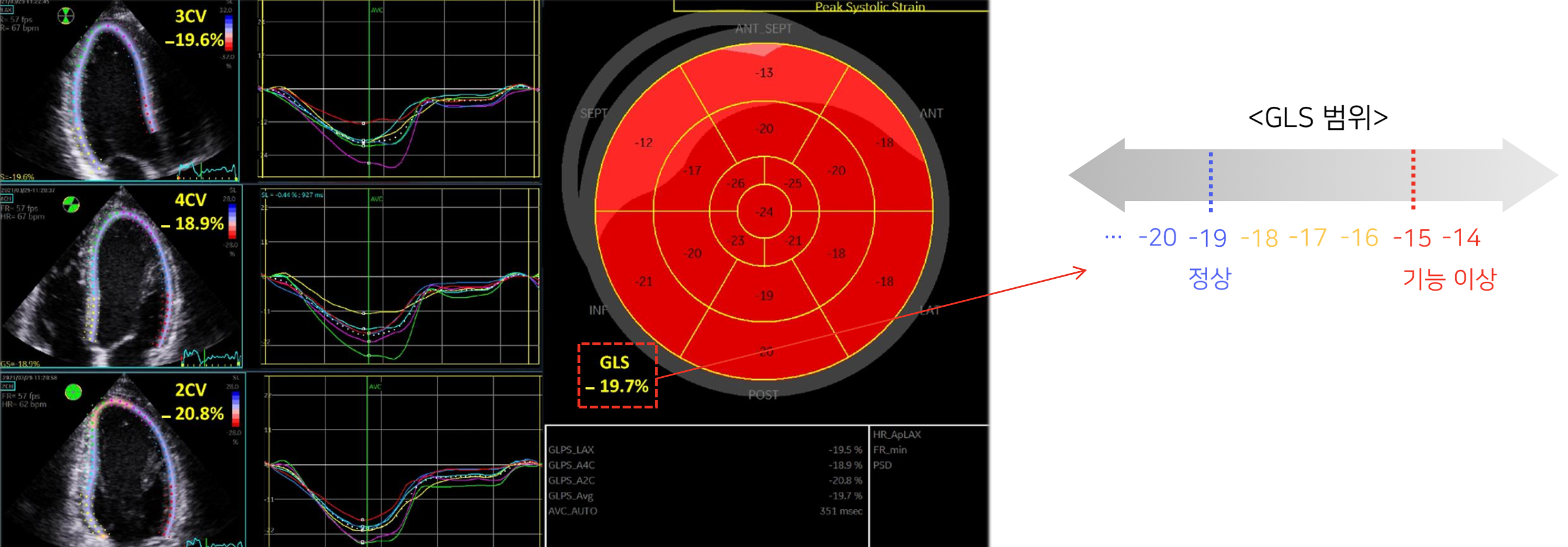
-GLS값은 -19를 기준으로 이하의 값으로 갈수록 (즉, -19, -20, -21 등) 정상이며, -15 이상으로 갈수록 (-15, -14, -13 방향으로) 심장의 수축 능력에 이상이 있다고 판단된다.
-다만 이 기준들은 고정적인 것은 아니고, 연령이나 성별 등에 따라 달라질 수 있다.
2.Methods
2-1. Study Flow
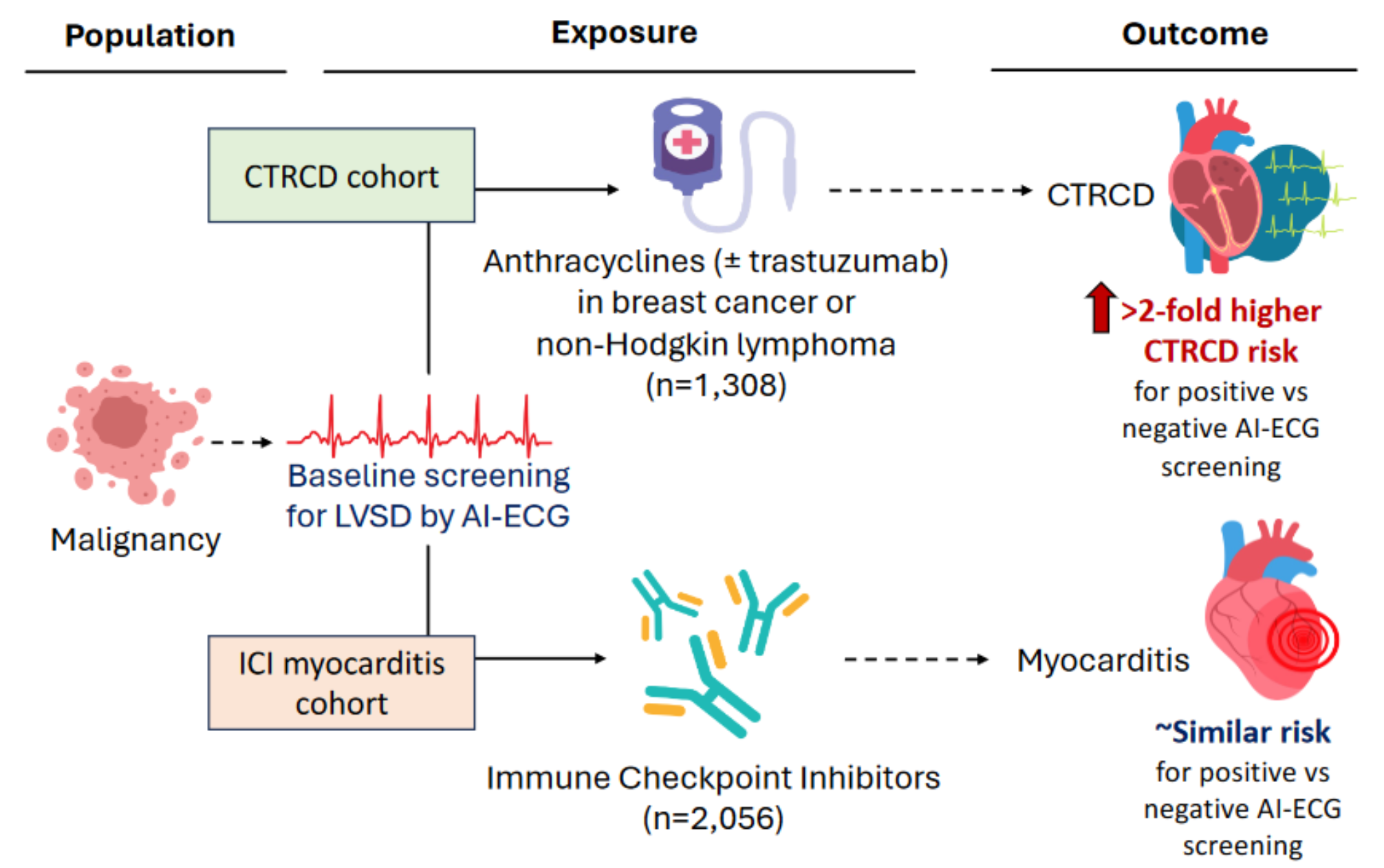
- 해당 연구는 총 2가지 코호트로 구성되었다.
- 안트라사이클린(약재 1), 트라스투주맙(약재 2), ICI(약재 3)로 항암 & 종양 치료를 받은 환자들을 대상으로 전체 population을 형성하고, 이 중, ICD-9 & 10 진단 코드를 활용하여 다시 두 개의 코호트로 분할하였다.
- CTRCD코호트의 경우, 유방암과 비호지킨 림프종 관련 진단을 받은 환자들 중, 암 진단 5년 이내에 안트라사이클린과 트라스투주맙 치료를 받은 18세 이상을 대상으로 한다.
- 그리고 이전에 해당 약물 치료를 받은 적이 있는 환자, LVEF가 50% 미만으로 떨어진 적이 있는 환자, cardiomyopathy, heart failure 병력이 있는 환자들은 제외되었다.
- ICI 코호트는 AI-ECG 모델의 특이성을 확인하기 위해 추가로 구성되었다. 즉, 이 연구에서는 AI-ECG 모델을 활용해서 CTRCD 발생을 예측하는 것이 주된 목표인데, 이 모델이 과연 다른 심장 문제에 대해서는 어떻게 작동하는지 확인하기 위해 해당 코호트가 추가로 구성된 것이다.
2-2. Study Covariates
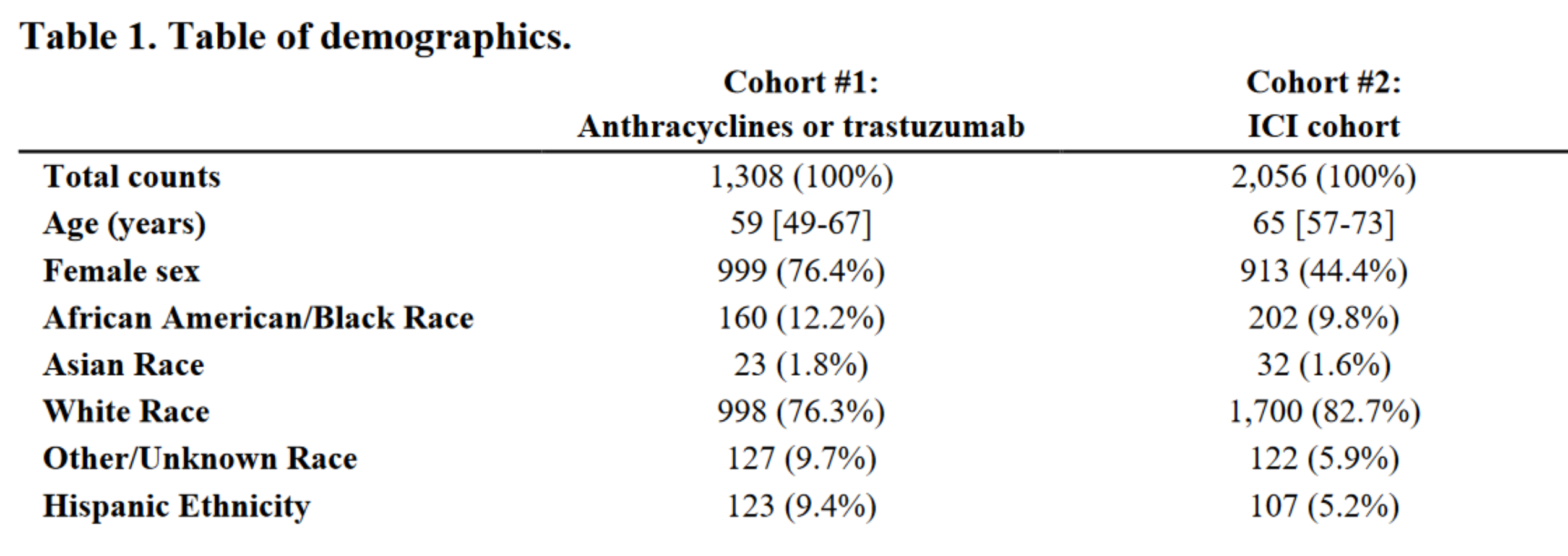
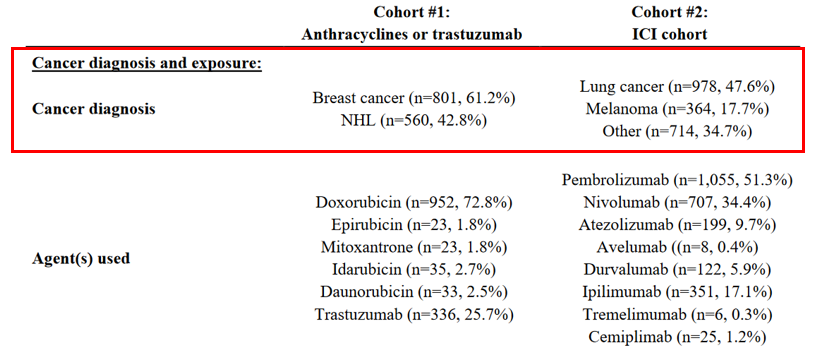
두 코호트는 각각 1,300명 그리고 2,000명으로 구성되었으며, 암 종별 비율을 보았을 때, 첫 번째 코호트의 경우 유방암과 비호지킨 림프종 환자들로만 구성되어있었고, 두번째 코호트의 경우 감암 환자가 가장 많은 비중을 차지했다.
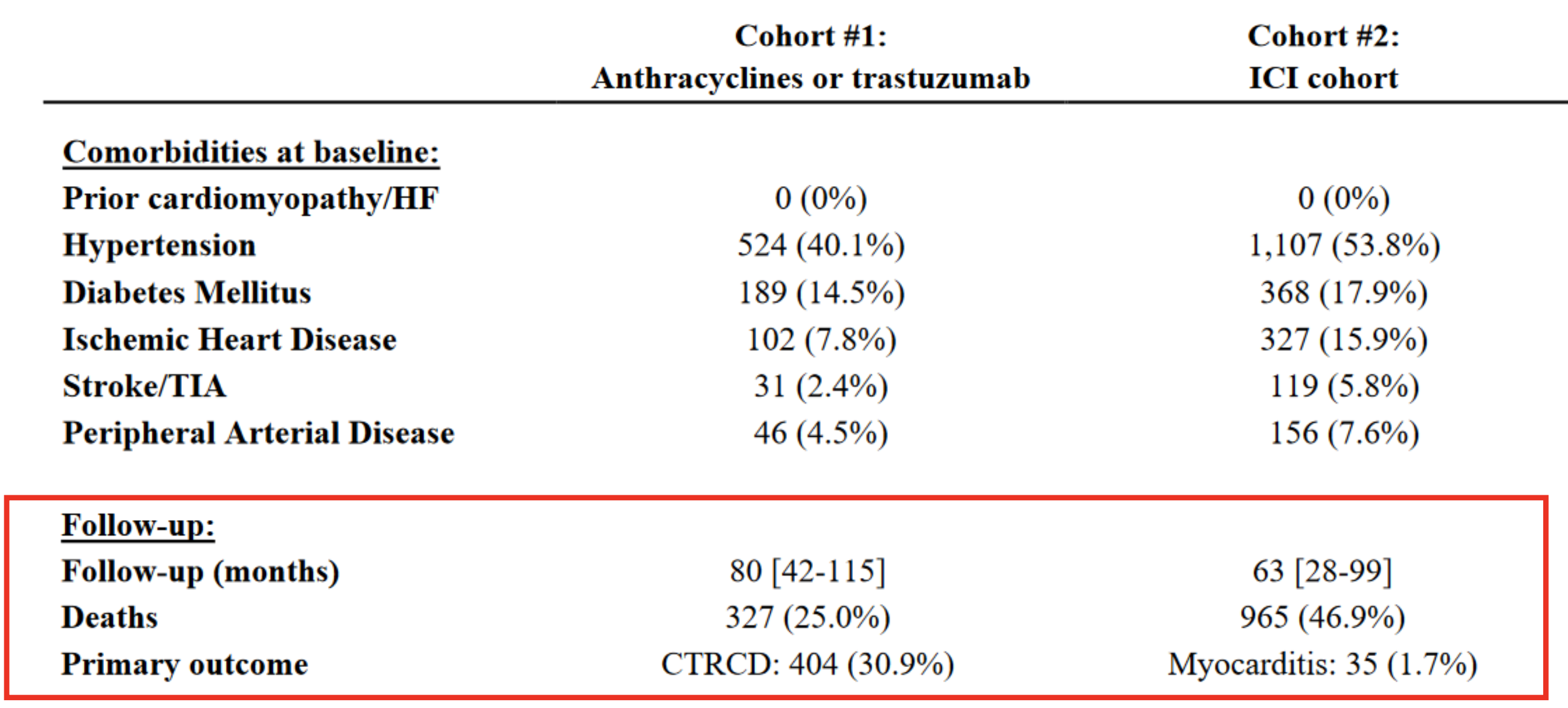
또한 첫번째 코호트는 평균 80개월 (약 6.6년)의 추적관찰 기간 동안 CTRCD 기준에 부합하는 사례는 약 30%, 두번째 코호트에서는 평균 63개월의 추적관찰 기간동안 Myocarditis가 발생된 케이스는 1%로 형성되었다.
2-3. Data source & Model
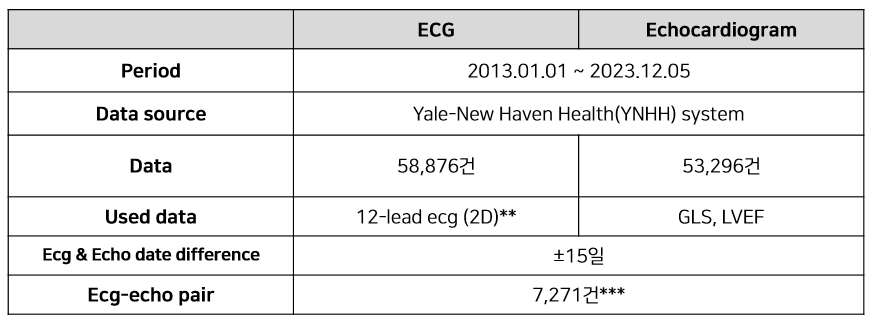
- 모든 데이터는 Yale Health System의 EHR에서 추출되었다.
- 심전도와 심장초음파 검사일 차이를 15일 이내로 설정했을 때, 약 7천 건의 데이터가 pair 되었다.
- 해당 데이터를 모델의 fine tuning에 활용되었다.
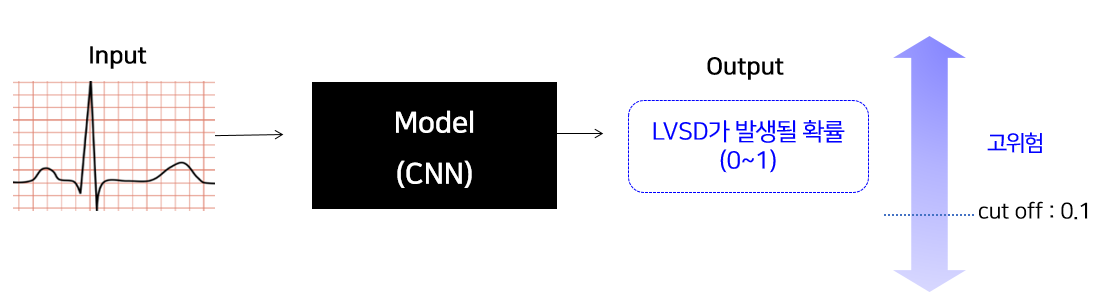
- 해당 연구에서는 이전에 검증된 CNN기반의 AI-ECG 모델을 활용하여 각 ECG 이미지 데이터에 대해 LVSD 발생 확률을 0~1 사이값으로 계산하였고, 이 예측값을 0.1을 기준으로 그 값 이상인 경우 LVSD위험이 높은 것으로 간주하였다.
3.Results
3-1. Cross-sectional correlation between AI-ECG and GLS
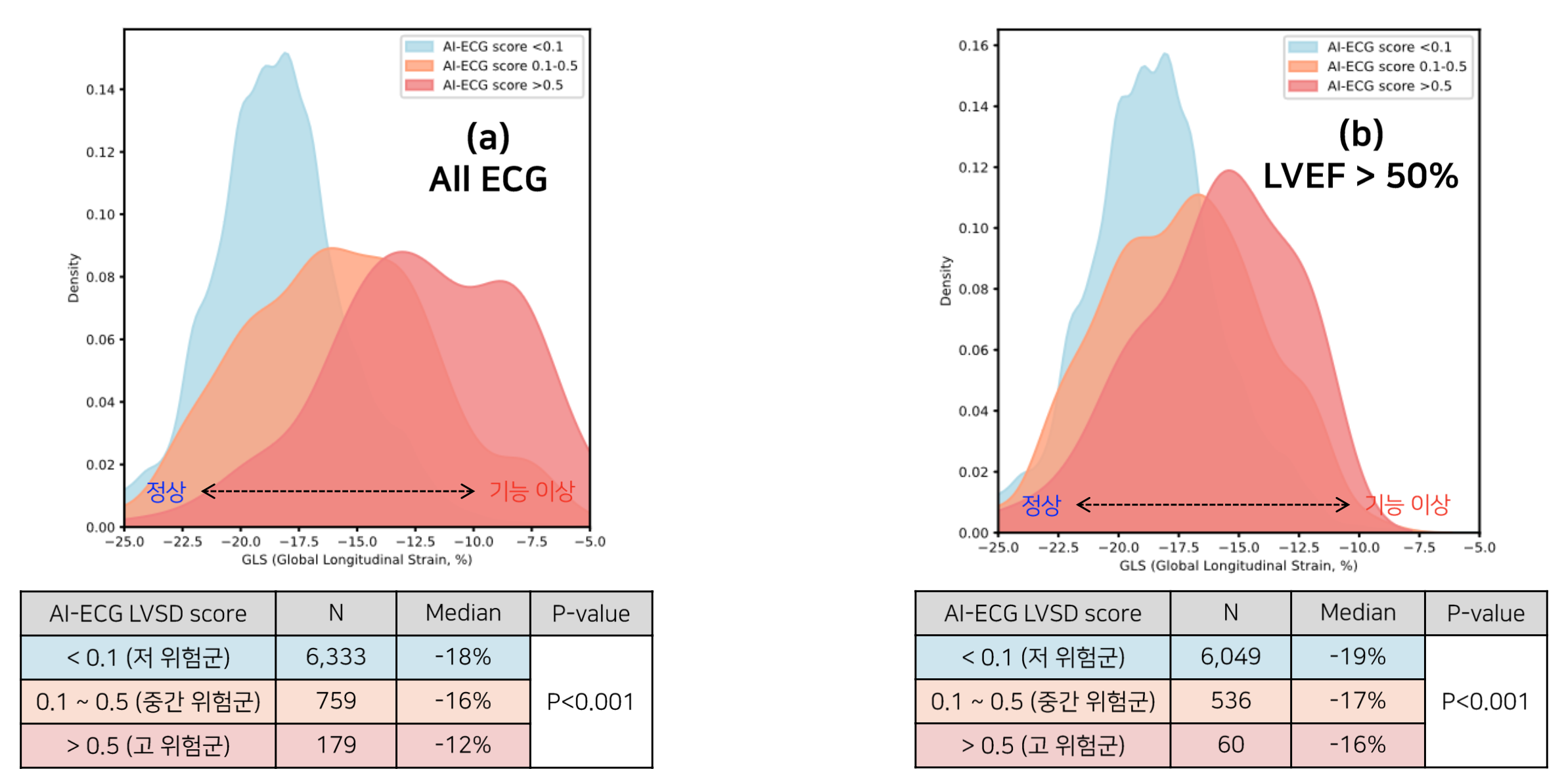
- AI-ECG에 의해 예측된 LVSD 발생 위험도에 따라 크게 세 그룹으로 분할하였다 (고위험군, 중간위험군, 저 위험군)
- 위의 그래프는 각 그룹별 같은 시점에서 측정한 (여기서는 +-15일 이내에 측정된) GLS값과의 correlation을 본 결과이다.
- 왼쪽 그래프를 기준으로 보았을 때, X축은 GLS값이며 왼쪽으로 갈수록 정상 오른쪽으로 갈수록 좌심실의 기능에 이상이 있음을 의미한다.
- 이때 AI- ECG모델이 LVSD 고위험군으로 예측한 경우(빨간색 그래프), GLS값도 다른 군들에 비해 0에 가까운 쪽에 분포해 있는 것을 확인하였다.
- 따라서 AI-ECG가 해당 환자를 LVSD위험 발생이 높은 것으로 예측한 경우, 실제로도 심장 기능에 이상이 발생되는 경향을 보이는 것을 의미한다.
3-2. AI-ECG and future CTRCD with anthracyclines and trastuzumab
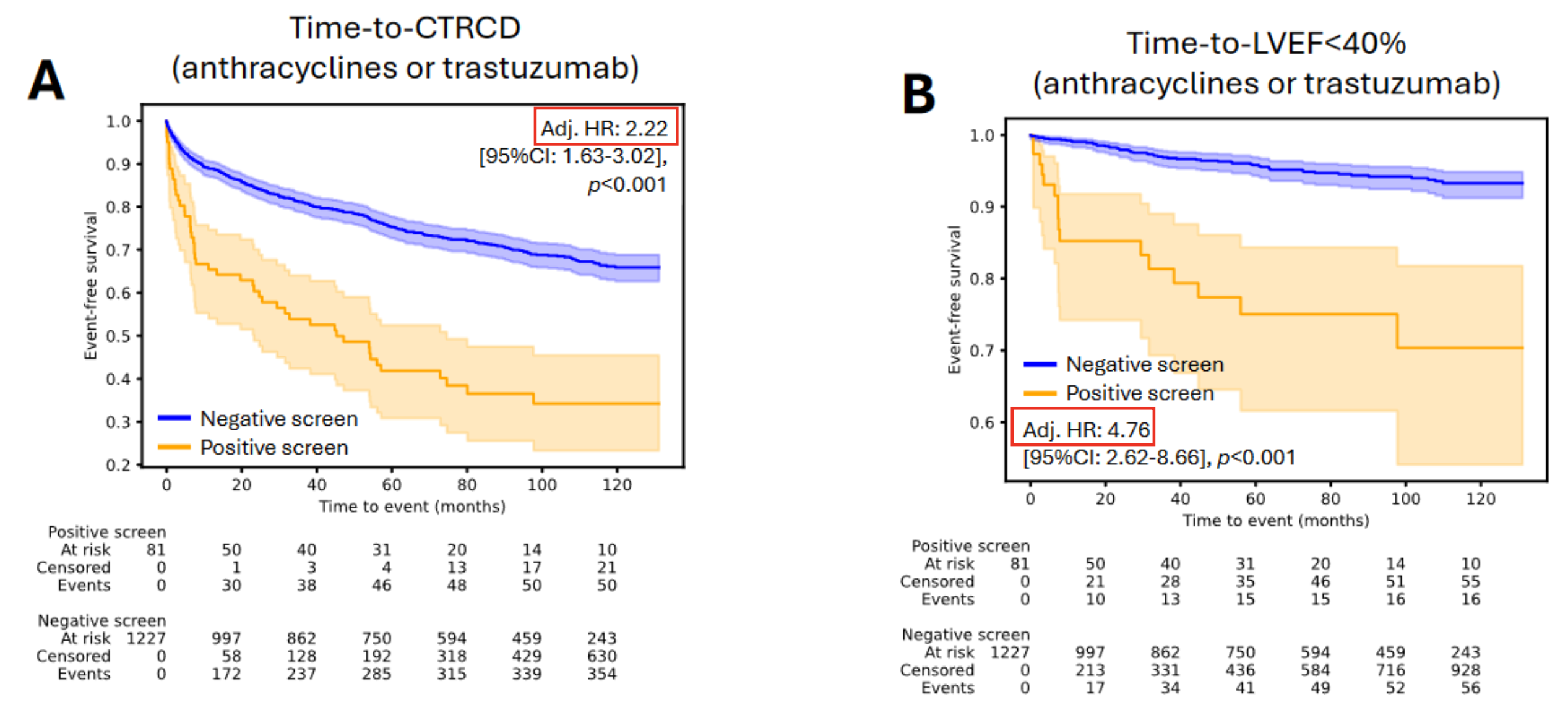
- 다음으로는, 안트라사이클린 또는 트라스투주맙 치료를 받은 환자들에서, Baseline 시점의 AI-ECG 스크리닝 결과에 따른 CTRCD 발생률을 비교한 그래프이다.
- 왼쪽 그래프에서, X축은 추적관찰기간, y축은 추적 관찰기간 동안 CTRCD 발생이 없는 환자의 비율을 의미한다.
- LVSD 위험이 높다고 예측되었을 때 (노란색 그래프), CTRCD가 발생될 확률이 2.22배 높게 나타났다.
3-3. Dynamic changes in AI-ECG LVSD prdictions prior to CTRCD
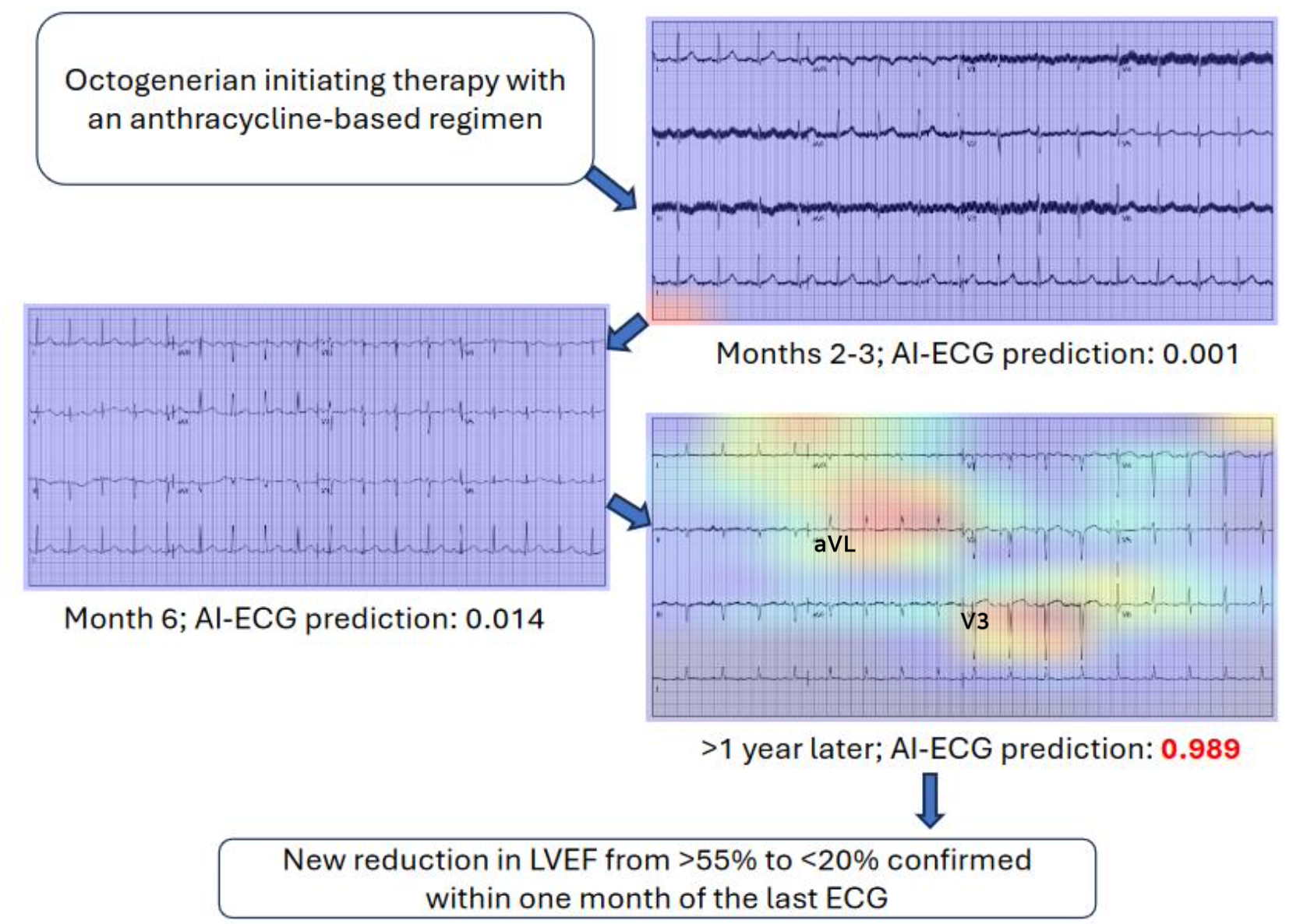
- 안트라사이클린 기반의 항암 치료를 받은 80세 환자에서, CTRCD가 진단되기까지 시간에 따른 AI-ECG의 LVSD 예측값 변화와 각 시점에서의 gradCAM을 시각화한 그래프이다.
- 해당 환자는 초기에 심장 관련 증상이 없었고, LVEF도 정상범위에 있었으며, 안트라 사이클린 약재로 치료 시작 후, 1년이 지난 시점에서 CTRCD로 진단되었다.
- 12개월 후 AI-ECG 예측값이 0.98로 매우 높게 나타났다.
- 이에 GradCAM을 확인해 보았을 때 V3, AVL리드 부분을 주목해서 해당 모델이 LVSD예측을 한 것을 알 수 있었고, 실제로도 ST-T 분절에서의 변화가 나타났다.
4. Disscusion & Conclusion
(3줄 요약)
- 심전도 기반 인공지능의 유용성 : 기존에는 심장 기능을 평가하기 위해 추로 심장 초음파가 사용되었으나, AI-ECG 모델은 심전도를 활용하여 더 간편하고 저렴한 비용으로 LVSD 및 CTRCD위험을 예측할 수 있음을 보여주었다.
- CTRCD 발생 고위험군의 조기 식별 가능성 : AI-ECG로 예측한 LVSD 고위험군에서는 실제로도 심장 기능의 저하가 더 자주 발견되었으며, 향후 CTRCD 발생 확률이 크게 높아지는 경향이 확인되었다.
- 일부 사례에서는 초기 심장 기능이 정상임에도 불구하고, 항암 치료 진행 중 AI-ECG 예측값이 동적으로 증가하여 심장 이상을 미리 감지할 수 있었다.